Kế hoạch bài dạy Hóa học Lớp 9 - Tiết 36: Luyện tập tính chất của bazơ - Năm học 2021-2022 - Trần Mạnh Hùng
Bạn đang xem tài liệu "Kế hoạch bài dạy Hóa học Lớp 9 - Tiết 36: Luyện tập tính chất của bazơ - Năm học 2021-2022 - Trần Mạnh Hùng", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Kế hoạch bài dạy Hóa học Lớp 9 - Tiết 36: Luyện tập tính chất của bazơ - Năm học 2021-2022 - Trần Mạnh Hùng
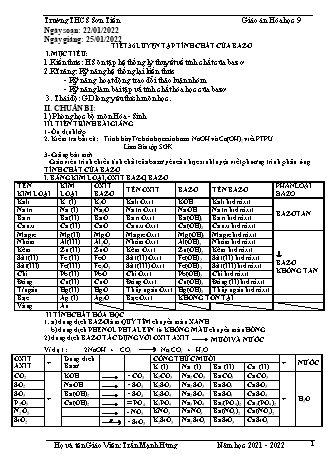
Trường THCS Sơn Tiến Giáo án Hóa học 9 Ngày soạn: 22/01/2022 Ngày giảng: 25/01/2022 TIẾT 36 LUYỆN TẬP TÍNH CHẤT CỦA BAZƠ I.MỤC TIÊU: 1.Kiến thức: HS ôn tập hệ thống lý thuyết về tính chất của baz ơ 2.Kĩ năng: Kỹ năng hệ thống lại kiến thức - Kỹ năng hoạt động trao đổi thảo luận nhóm - Kỹ năng làm bài tập vầ tính chất hóa học của bazơ 3. Thái độ: GD lòng yêu thích môn học. II. CHUẨN BỊ: 1) Phòng học bộ môn Hóa - Sinh III. TIẾN TRÌNH BÀI GIẢNG. 1- Ổn định lớp 2. Kiểm tra bài cũ: Trình bày T/c hóa học của bazơ NaOH và Ca(OH)2 viết PTPƯ Làm Bài tập SGK 3- Giảng bài mới Giáo viên trình chiếu tính chất của bazơ yêu cầu học sinh luyện viết phương trình phản ứng TÍNH CHẤT CỦA BAZƠ I. BẢNG KIM LOẠI, OXIT BAZƠ, BAZƠ TÊN KIM OXIT PHÂN LOẠI TÊN OXIT BAZƠ TÊN BAZƠ KIM LOẠI LOẠI BAZƠ BAZƠ Kali K (I) K2O Kali Oxit KOH Kali hiđrôxit Natri Na (I) Na O Natri Oxit NaOH Natri hiđrôxit 2 BAZƠ TAN Bari Ba (II) BaO Bari Oxit Ba(OH)2 Bari hiđrôxit Canxi Ca (II) CaO Canxi Oxit Ca(OH)2 Canxi hiđrôxit Magie Mg(II) MgO Magie Oxit Mg(OH)2 Magie hiđrôxit Nhôm Al(III) Al2O3 Nhôm Oxit Al(OH)3 Nhôm hiđrôxit Kẽm Zn (II) ZnO Kẽm Oxit Zn(OH)2 Kẽm hiđrôxit Sắt (II) Fe (II) FeO Sắt (II) Oxit Fe(OH) Sắt (II) hiđrôxit 2 BAZƠ Sắt(III) Fe(III) Fe O Sắt (III) Oxit Fe(OH) Sắt (III) hiđrôxit 2 3 3 KHÔNG TAN Chì Pb (II) PbO Chì Oxit Pb(OH)2 Chì hiđrôxit Đồng Cu(II) CuO Đồng Oxit Cu(OH)2 Đồng (II) hiđrôxit T/ngân Hg(II) HgO Thủy ngân Oxit Hg(OH)2 Thủy ngân hiđrôxit Bạc Ag (I) Ag2O Bạc Oxit KHÔNG TỒN TẠI Vàng Au II TÍNH CHẤT HÓA HỌC 1. a) dung dịch BAZƠ làm QUỲ TÍM chuyển màu XANH b) dung dịch PHENOL PHTALEIN từ KHÔNG MÀU chuyển màu HỒNG 2) dung dịch BAZƠ TÁC DỤNG VỚI OXIT AXIT MUỐI VÀ NƯỚC Ví dụ 1: 2NaOH + CO2 Na2CO3 + H2O OXIT Dung dich CÔNG THỨC MUỐI + + NƯỚC AXIT Bazơ K (I) Na (I) Ba (II) Ca (II) CO2 KOH = CO3 K2CO3 Na2CO3 BaCO3 CaCO3 SO2 NaOH = SO3 K2SO3 Na2SO3 BaSO3 CaSO3 SO3 Ba(OH)2 = SO4 K2SO4 Na2SO4 BaSO4 CaSO4 + + H2O P2O5 Ca(OH)2 PO4 K3PO4 Na3PO4 Ba3(PO4)2 Ca3(PO4)2 N2O5 - NO3 KNO3 NaNO3 Ba(NO3)2 Ca(NO3)2 t0 SiO2 = SiO3 K2SiO3 Na2SiO3 BaSiO3 CaSiO3 Họ và tên Giáo Viên: Trần Mạnh Hùng Năm học 2021 - 2022 1 Trường THCS Sơn Tiến Giáo án Hóa học 9 Chú ý 1: với CO2/ SO2 tác dụng với NaOH/KOH thì theo tỉ lệ số mol sẽ có sản phẩm khác nhau Chú ý 2: với CO2/ SO2 tác dụng với Ba(OH)2/Ca(OH)2 thì theo tỉ lệ số mol sẽ có sản phẩm khác nhau 3) BAZƠ TÁC DỤNG VỚI AXIT MUỐI VÀ NƯỚC Ví dụ 1: Fe(OH)3 + 3HCl FeCl3 + 3H2O TÊN KIM OXIT KIM BAZƠ + AXIT Gốc MUỐI + NƯỚC LOẠI BAZƠ LOẠI Khi Kali K (I) K2O KOH H2S =S Sunfua Nào Natri Na (I) Na2O NaOH H2CO3 =CO3 Cácbônát Bạn Bari Ba (II) BaO Ba(OH)2 H2SO3 =SO3 Sunfít Cần Canxi Ca (II) CaO Ca(OH)2 H2SO4 =SO4 Sunfát Mua Magie Mg(II) MgO Mg(OH)2 HNO3 -NO3 Nitrát Áo Nhôm Al(III) Al2O3 Al(OH)3 HNO2 NO2 Nitrít Záp Kẽm Zn (II) ZnO Zn(OH)2 + H3PO4 PO4 Phốt phát + H2O Sắt Sắt (II) Fe (II) FeO Fe(OH)2 HCl -Cl Clorua Sắt Sắt(III) Fe(III) Fe2O3 Fe(OH)3 HClO3 -ClO3 Clorát Phải Chì Pb (II) PbO Pb(OH)2 HBr - Br Brômmua Cửa Đồng Cu(II) CuO Cu(OH)2 HF - F Florua Hàng T/ngân Hg(II) HgO Hg(OH)2 Á Bạc Ag (I) Ag2O 4) BAZƠ KHÔNG TAN BỊ NHIỆT PHÂN TẠO OXIT BAZƠ VÀ NƯỚC t0 Ví dụ 1: Cu(OH)2 CuO + H2O 0 TÊN BAZƠ BAZƠ t + NƯỚC Magie hiđrôxit Mg(OH)2 MgO Nhôm hiđrôxit Al(OH)3 Al2O3 Kẽm hiđrôxit Zn(OH)2 ZnO Sắt (II) hiđrôxit Fe(OH)2 t0 FeO + H2O Sắt (III) hiđrôxit Fe(OH)3 Fe2O3 Chì hiđrôxit Pb(OH)2 PbO Đồng (II) hiđrôxit Cu(OH)2 CuO Thủy ngân hiđrôxit Hg(OH)2 HgO Chú ý: - nếu Fe(OH)2 bị nhiệt phân không có oxi tạo thành Sắt (II) oxit t0 Fe(OH)2 FeO + H2O - nếu Fe(OH)2 bị nhiệt phân có oxi (trong không khí) tạo thành Sắt (III) oxit t0 PTPƯ: 4Fe(OH)2 + O2 2Fe2O3 + 4H2O 5) dung dịch BAZƠ tác dụng với dung dịch MUỐI BAZƠ mới + MUỐI mới 5.1 dung dịch bazơ tác dụng với dung dịch muối tạo thành muối mới và bazơ mới kết tủa Ví dụ 1: NaOH + CuSO4 Cu(OH)2 + Na2SO4 Dung dich + Dung dịch muối của các KIM LOẠI Bazơ KOH NaOH + Mg (II) Al (II) Zn (II) Fe (II) Fe (III) Pb(II) Cu(II) Hg(II) Ag(I) Ba(OH)2 Ca(OH)2 Ag O TẠO THÀNH BAZƠ MỚI KẾT TỦA M(OH)n VÀ MUỐI MỚI 2 + H2O 2 Họ và tên Giáo Viên: Trần Mạnh Hùng Năm học 2021 - 2022 Trường THCS Sơn Tiến Giáo án Hóa học 9 5.2 dung dịch bazơ tác dụng với dung dịch muối tạo thành muối mới kết tủa và bazơ mới Ví dụ 1: Ba(OH)2 + Na2SO3 2NaOH + BaSO3 Dung dich + Dung dịch muối của các GỐC AXIT Bazơ Ba(OH)2 + = CO3 =SO3 =SO4 PO4 BAZƠ Tạo thành muối BaCO BaSO BaSO Ba (PO ) + 3 3 4 3 4 2 mới Dung dich + Dung dịch muối của các GỐC AXIT Bazơ Ca(OH)2 + = CO3 =SO3 =SO4 PO4 =S + BAZƠ Tạo thành muối CaCO CaSO CaSO Ca (PO ) CaS 3 3 4 3 4 2 mới Ví dụ 1: 2NaOH + CO2 Na2CO3 + H2O OXIT Dung dich CÔNG THỨC MUỐI + + NƯỚC AXIT Bazơ K (I) Na (I) Ba (II) Ca (II) CO2 KOH = CO3 K2CO3 Na2CO3 BaCO3 CaCO3 SO2 NaOH = SO3 K2SO3 Na2SO3 BaSO3 CaSO3 SO3 Ba(OH)2 = SO4 K2SO4 Na2SO4 BaSO4 CaSO4 P2O5 + Ca(OH)2 PO4 K3PO4 Na3PO4 Ba3(PO4)2 Ca3(PO4)2 + H2O N2O5 - NO3 KNO3 NaNO3 Ba(NO3)2 Ca(NO3)2 SiO t0 K SiO Na SiO BaSiO CaSiO 2 = SiO3 2 3 2 3 3 3 I. Giáo viên trình chiếu tính chất của bazơ yêu cầu học sinh luyện viết phương trình phản ứng và ghi chép II bài tập vận dụng Gv chia lớp thành hai nhóm tiến hành 1) (1) (2) (3) (4) (5) (6) a) Cu CuO CuCl2 Cu(OH)2 CuO Cu CuSO4. (1) (2) (3) (4) (5) b) Na Na2O NaOH Na2SO4 NaCl NaNO3 2): Cho các chất sau: Fe, Fe(OH)3 , FeCl3 , Fe2O3 , Fe2(SO4)3 hãy sắp xếp thành một chuỗi phản ứng và viết phương trình phản ứng để hoàn thành chuỗi đó. 3): Từ các chất: CaO, Na2CO3 và H2O, viết PTHH điều chế dd NaOH. 4) : Từ những chất: Na2O, BaO, H2O, dd CuSO4, dd FeCl2, viết các PTHH điều chế: dd NaOH. dd Ba(OH)2. BaSO4. Cu(OH)2. Fe(OH)2 Giáo viên vừa trình chiếu kiến thức bài tập yêu Học sinh hoạt động theo nhóm và hoàn thành cầu học sinh trình bà Học sinh nhóm còn lại bổ sung và ghi kết quả G/V yêu cầu nhóm còn lại bổ sung và chốt kiến đúng thức 4. CỦNG CỐ, ĐÁNH GIÁ Giáo viên đánh giá nhận xét trong quá trình học tập chủ đề bazơ 5. DẶN DÒ BTVN: SGK Họ và tên Giáo Viên: Trần Mạnh Hùng Năm học 2021 - 2022 3
File đính kèm:
 ke_hoach_bai_day_hoa_hoc_lop_9_tiet_36_luyen_tap_tinh_chat_c.doc
ke_hoach_bai_day_hoa_hoc_lop_9_tiet_36_luyen_tap_tinh_chat_c.doc

